PDGF(B)/v-sis: механизм трансформации
Следующим шагом после обнаружения гомологии между v-sis и PDGF-B было открытие их функционального сходства. Так, выделенный из зараженных SSV клеток v-sis конкурировал с меченым PDGF за места связывания на поверхности клетки. Кроме того, v-sis оказался способным вызывать фосфорилирование и активацию PDGF-R ( Leal et al 1985 ). Описанные эффекты исчезали при добавлении антител к PDGF-BB или PDGF-R ( Johnsson A. ea, 1985 ).
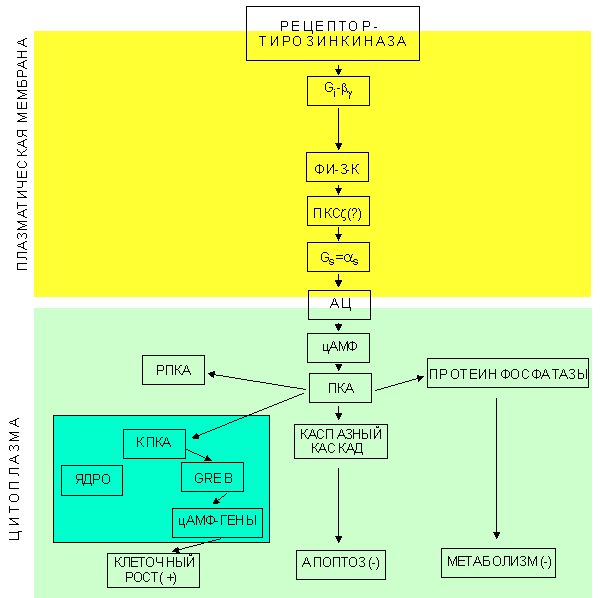
Ингибирование транформации при добавлении в среду антител к фактору или его рецептору говорит о том, что для достижения эффекта белок должен пройти все стадии посттрансляционной модификации и покинуть клетку: однако было показано, что v-sis способен активировать тирозинкиназу рецептора PDGF находясь еще внутри клетки ( Keating M.T. and Williams L.T., 1988 ). При суммировании всех полученных результатов была выдвинута гипотеза о том, что, действительно, переход рецепторов в активированное состояние может иметь место еще в аппарате Гольджи в течение процессинга белков. Однако для запуска митогенного сигнала комплекс рецептор-лиганд должен появиться на поверхности клетки; активированный внутриклеточно рецептор не способен индуцировать полноценный клеточный ответ ( рис.1. Механизм воздействия на клетку v-sis/PDGF-B ) ( Heldin C.-H. and Westermark B., 1989 ).
В связи с этим уместно вспомнить, что по крайней мере два участника цепи передачи сигнала PDGF внутрь клетки ( p21ras и протеинкиназа С ) являются примембранными белками , т.е. расположены с внутренней стороны плазматической мембраны. Вероятно, этим можно объяснить тот факт, что при нарушении внутриклеточного везикулярного транспорта в зараженных клетках не наблюдалося повышения уровня транскрипции гена c-fos , характерного для PDGF-индуцированного митогенеза ( Hannink M. and Donoghue D.J., 1988 , цит. по Heldin C.-H. and Westermark B., 1989 ).
Смотрите также: