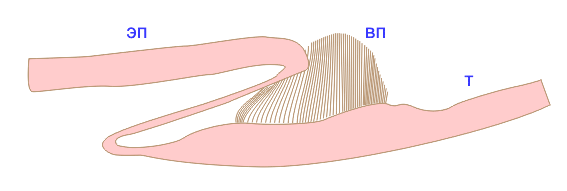
Регуляция прокариот на экстремальные условия
Прокариоты реагируют на экстремальные условия комплексом изменений развития.
Основные положения:
- Прокариоты реагируют на такие экстремальные условия, как голодание, многочисленными адаптивными изменениями.
- Простейшие из этих изменений затрагивают процессы генной экспрессии и метаболизма, а также замедление прохождения клетки по циклу, тем самым подготавливая ее к периоду голодания.
- В некоторых случаях голодание приводит к появлению таких высокодифференцированных и специализированных клеток, как эндоспоры Bacillus subtilis .
- В условиях голодания такие микроорганизмы, как актиномицеты , образующие мицелий , характеризуются сложной морфологией колоний и продуцируют воздушные гифы , споры и вторичные метаболиты.
- Межклеточная кооперация и развитие бактерий хорошо иллюстрируются на примере Myxococcus xanthus .
Для многих популяций прокариот при наличии питательных компонентов характерны периоды быстрого роста, которые при недостатке питания или при накоплении токсических метаболитов сменяются снижением его темпов или приостановкой. В некоторых случаях прокариоты реагируют на голодание, просто регулируя соответствующие метаболические процессы. Частично эта регуляция осуществляется за счет изменений экспрессии генов, в результате чего ресурсы перенаправляются на участие в процессах, необходимых для выживания клеток, а не для их роста. Иногда в клетках происходят сложные процессы дифференцировки с участием двух и более отдельных типов дифференцированных клеток.
Например, наступление стационарной фазы в клетках Е. coli вызывает изменение экспрессии множества генов. Эти изменения происходят в ответ на определенные метаболические стимулы и зависят от природы сигнала, который генерируется в клетке при наступлении голодания. Иногда эти изменения ограничиваются наступлением периода ограниченного роста клеток. Однако, когда исчерпаны все возможности, в клетках развивается более общий ответ на голодание, который, главным образом, контролируется специальным сигма-фактором сигма^S , представляющим собой субъединицу РНК-полимеразы, продукт гена rpoS . Как следует из рис. 20.46 , сигма^S подвергается целому ряду регулирующих воздействий, действующих на уровне транскрипции и трансляции, а также на посттрансляционном уровне. Увеличение количества белка сигма^S может достигаться или за счет стимуляции его синтеза на уровне транскрипции гена rpoS, или на уровне трансляции мРНК , а также за счет ингибирования его протеолиза (в обычных, неэкстремальных условиях протеолиз происходит чрезвычайно быстро). Наиболее быстрый и эффективный ответ клетки, например при гиперосмотическом шоке или при сдвиге рН, достигается за счет комбинации перечисленных процессов. Такая комплексная регуляция позволяет клетке вырабатывать единообразный ответ на воздействие самых разных экстремальных факторов.
Под контролем сигма^S находится большое количество генов. На рис. 20.47 перечислены некоторые из числа наиболее исследованных, и указаны их функции, обеспечивающие адаптацию клеток к условиям, не способствующим их росту. В результате наступления стационарной фазы, клетки переходят в фазу покоя, в которой они проявляют высокую устойчивость к экстремальным внешним факторам, несовместимым с жизнедеятельностью растущих клеток
В отличие от Е. coli, реакция клеток В. subtilis на отсутствие питательных компонентов проявляется в споруляции , т.е. в процессе образования спор (латентных клеток) ( рис. 20.48 ). У В. subtilis споры развиваются в бактериях, в виде эндоспор . Переход от вегетативной фазы роста к споруляции находится под сложным контролем более двух десятков регуляторных генов, активность которых зависит от многих внутри- и внеклеточных факторов. Ключевыми положительными регуляторами экспрессии генов, участвующих в споруляции, являются сигма-фактор сигма^H и регулятор Spo0A . Последний белок активируется при фосфорилировании , и доставка фосфатных групп на Spo0A является ключевым моментом и осуществляется с помощью, по крайней мере, двух киназ , двух промежуточных переносчиков фосфатных групп, и трех или более фосфатаз . Все эти ферменты способны активировать или блокировать процесс споруляции. Наряду с положительной системой регуляции, многие репрессоры транскрипции способны снижать экспрессию ключевых генов регуляторного аппарата.
Три группы фактов указывают на то, что эта сложная регуляторная система находится в клетке в состоянии постоянного мониторинга.
- Во-первых, вероятно, что к числу основных принадлежат сигналы, связанные с наличием питательных компонентов. При этом одним из ведущих индикаторов служит уровень ГТФ . В этой системе регуляции основная роль принадлежит белку CodY , связывающему ГТФ.
- Во-вторых, клетки получают информацию о плотности растущей популяции посредством системы quorum sensing , которая следит за уровнем накопления во внешней среде секретируемого пептида (подробнее о quorum sensing см. Биопленки представляют собой высокоорганизованные сообщества микробов ). Только при высокой плотности клеточной популяции концентрация пептида достигает достаточно высокого для начала споруляции уровня.
- В-третьих, критическую роль в инициации споруляции играет положение клетки в цикле, и это событие может происходить только в том случае, когда клетки находятся в определенной его точке. В противном случае наступает еще один цикл деления. Наряду с этим, при нарушениях репликации или сегрегации хромосом, различные контрольные точки предотвращают наступление споруляции.
Инициация споруляции приводит к модификации асимметричного клеточного деления ( рис. 20.48 ). Переключение на асимметричное деление, очевидно, происходит за счет увеличения уровня белка FtsZ и синтеза специфического белка SpoIIE , хотя неизвестно, как конкретно эти белки осуществляют переключение. Это критическая точка процесса развития, поскольку образуются два разных типа клеток, которые затем, при формировании спор, функционируют совместно. Небольшие клетки преспоры предназначены для превращения в зрелые эндоспоры. Гораздо большая по размеру материнская клетка все свои ресурсы расходует на созревание споры. Такой кооперативный подход обусловливает высокую выживаемость бактерий, образующих эндоспоры, поскольку эндоспоры гораздо прочнее и более устойчивы по сравнению со специализированными клетками, для которых характерен подход "каждый за себя". Устойчивость определяется комбинацией факторов, включая дегидратацию и минерализацию спорового кора и образование наружных защитных слоев, называемых кортексом (модифицированная форма клеточной стенки) и белковая оболочка. Сложная программа экспрессии генов, которая реализуется в преспоре В. subtilis и в материнской клетке, в настоящее время подробно исследована.
Еще одна грамположительная бактерия, Streptomyces coelicolor , характеризуется более сложной системой ответа на отсутствие питательных компонентов. Этот микроорганизм относится к актиномицетам и, подобно филаментозным грибам, растет в виде ветвящихся нитей. В отличие от таких свободно живущих бактерий, как Е. coli и В. subtilis, при голодании S. coelicolor почти неизбежно начинает расти в виде сети (мицелия), состоящей из филаментов, называемых гифами . Как показано на рис. 20.49 , развитие колонии начинается с формирования субстратного мицелия, который разрастается по поверхности ростовой среды (почвы). В теле колонии гифы голодают, в то время как на периферии бурно растут. В ответ на отсутствие питательных компонентов, образуются специальные воздушные гифы, которые растут вертикально вверх от поверхности колонии. Хотя гифы субстратного мицелия характеризуются незначительным количеством перегородок деления, в воздушных гифах деление сильно интенсифицируется, что приводит к образованию массы одноядерных клеток, которые дифференцируются в устойчивые споры. Опять-таки, инициация развития воздушных гиф и спор происходит с участием сложного набора регулирующих факторов (даже более сложных, чем в случае В. subtilis). Жизненный цикл актиномицетов очень важен с промышленной точки зрения, поскольку примерно при переходе от растущего мицелия к среде с недостатком продуктов питания эти организмы продуцируют ряд полезных вторичных метаболитов. Среди них особенно ценными являются антибиотики , которые, вероятно, подавляют деятельность конкурирующих бактерий, содержащихся в почве.
Одним из наиболее ярких примеров, иллюстрирующих процесс развития у микроорганизмов, являются миксобактерии . К числу наиболее изученных представителей этой группы относятся Myxococcus xanthus . Как следует из рис. 20.50 и рис. 20.51 , при недостатке в питательных компонентах, клеточная популяция собирается в локальные группы клеток. В эти группы объединяется много клеток, которые образуют крупные конгломераты. Когда палочковидные клетки округляются и дифференцируются в миксоспоры , эти конгломераты превращаются в плодовые тела, находящиеся в латентной форме и устойчивые к обезвоживанию. Некоторые миксобактерии, такие как Stigmatella , образуют комплекс плодоносящих тел со множественными спорангиолами , расположенными на ветвящихся ножках.
У Myxococcus xanthus, так же как у В. subtilis, идентифицировано много генов, принимающих участие в процессе развития. Наиболее важные вопросы, относящиеся к проблеме развития микроорганизмов, которые можно исследовать на этой бактерии, относятся к процессам межклеточной передачи сигнала . На разных этапах развития происходит обмен межклеточными сигналами, что способствует агрегации и морфогенезу плодовых тел. При генетическом анализе мутантов с нарушенной функцией передачи межклеточных сигналов, были идентифицированы сигнальные системы, две из которых, обозначенные сигнальная система A и сигнальная система C , в настоящее время исследованы достаточно подробно. Сигнальная система A принимает участие на раннием этапе развития и представляет собой сложный набор аминокислот, которые образуются при действии одной или нескольких клеточных протеаз. Этот сигнал, по-видимому, используется для оценки общей обеспеченности клеточной популяции питательными компонентами. На рис. 20.52 представлены некоторые молекулярные механизмы, контролирующие процессы генерации и восприятия сигнала. Сигнальная система C начинает функционировать на более поздних этапах ( рис. 20.53 ). Сигнал, характерный для этой системы, предполагает наличие тесного контакта между двумя клетками. Фактор C представляет собой белок величиной 25 кДа, связанный с поверхностью клетки. По свойствам он близок к семейству небольших алкогольдегидрогеназ . Ферментная функция этого белка неизвестна. Для обмена сигналами клетки должны проявлять подвижность. Это связано с тем, что сигнал проходит только через концы клеток, и, поэтому, они должны сориентироваться в правильной позиции друг к другу. Молекулярные механизмы передачи сигнала неизвестны, однако система представляет большой интерес для понимания основ развития многоклеточности.
Смотрите также: