Коллагены фибрилообразующе: самосборка
Самосборка фибрилообразующих коллагенов в течение многих лет исследовалась с помощью нагревания и нейтрализации растворов коллагенов, экстрагированных из тканей холодными кислотными буферами [ Prockop ea 1994 , Veis ea 1994 ]. Позже процесс был исследован в системе с pC-коллагеном , растворимым и частично преобразованным предшественником с отсутствующим N-концевым пропептидом, расщепляемым до коллагена очищенной C-протеиназой проколлагена в физиологическом буфере в физиологическом диапазоне температур [ Prockop ea 1994 ]. Расщепление pC-коллагена до коллагена сопровождается снижением растворимости белка приблизительно в 1000 раз. В конечном итоге коллаген самоорганизуется в плотно "упакованные" фибриллы [ Prockop ea 1994 , Kadler ea 1987 ].
Была проведена серия экспериментов по выделению проколлагена I-го типа и его расщеплению C-протеиназой для образования pN-коллагена I-го типа [ Prockop ea 1994 ]. PN-коллаген собран в тонкие поперечнополосатые листоподобные структуры одинаковой толщины. Смеси коллагена I-го типа и pN-коллагена кополимеризовались, образуя разнообразные плеоморфные фибриллы. Результаты соответствовали предположению, согласно которому при определенных обстоятельствах pN-коллаген I-го типа осуществляет изменение морфологии фибрилл коллагена I-го типа [ Prockop ea 1994 , Romanic ea 1992 ].
PN-коллаген III-го типа также образовывал истинные кополимеры с коллагеном I-го типа, и в результате кополимеризации возникали более тонкие фибриллы, нежели те, что образованы собственно коллагеном I-го типа [ Romanic ea 1991 ]. Результаты сответствовали модели, согласно которой pN- коллаген III-го типа способен регулировать диаметр фибрилл коллагена I- го типа, покрывая их поверхность [ Romanic ea 1991 ].
В сходных экспериментах рекомбинантный pC-коллаген II-го типа был использован для образования фибрилл посредством инкубации с C- протеиназой [ AlaKokko ea 1991 ]. Кинетика сборки фибрилл коллагена II-го типа существенно отличалась от таковой для коллагена I-го типа, причем критическая концентрация при 37 C была приблизительно в 50 раз выше. Кроме того, фибриллы коллагена II-го типа были относительно тонкими и образовывали трехмерные сети.
Результаты указывают на то, что различия первичных структур коллагенов I-го и II-го типов достаточно для объяснения многих характерных морфологических различий между двумя указанными разновидностями обнаруженных в тканях фибрилл [ Fertala ea 1994 ].
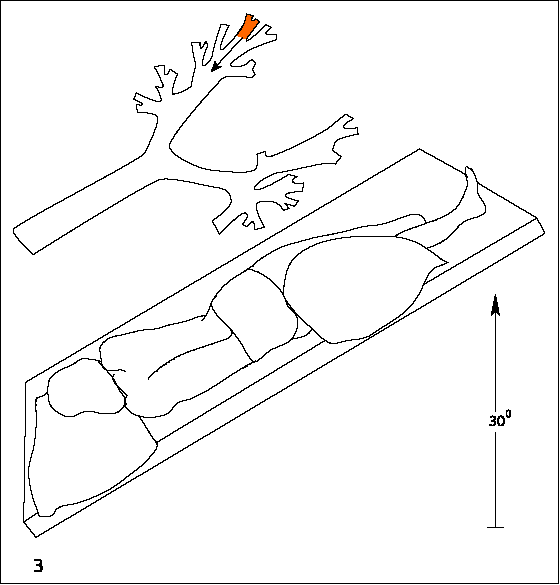
Система создания фибрилл коллагена I-го типа посредством ферментативного расщепления pC-коллагена сделала возможным исследование роста фибрилл, начиная с промежуточных стадий. Первые обнаруженные фибриллы обладали тупым концом и заостренной верхушкой [ Holroes ea 1992 ]. Первичный рост фибриллы начинался исключительно с заостренной верхушки. На более поздней стадии верхушки образовывались на тупых концах и фибриллы росли в обоих направлениях. Как первичные верхушки, так и верхушки более поздних стадий обладали формой, близкой к параболической [ Holroes ea 1992 ].
На основании подобных наблюдений была создана модель роста фибриллы [ Silver ea 1992 ], в качестве существенной особенности которой предполагается наличие характерного структурного ядра, формируемого на каждом конце растущей фибриллы. Затем рост фибриллы происходит в результате расширения обоих структурных ядер. Структурные ядра обладают сходными спиральными конформациями, причем для сборки и расширения каждого структурного ядра необходимы два типа стадий специфического связывания [ Silver ea 1992 ].
Аналогичные исследования фибрилл рекомбинантного коллагена II-го типа показали, что верхушки также обладали формой, близкой к параболической [ Fertala ea 1994 ъ. Однако, мономеры верхушек двух типов ориентированы различным образом. В верхушках фибрилл коллагена I-го типа все мономеры были ориентированы таким образом, чтобы N-концы были указывали на окончание верхушки [ Holroes ea 1992 ]. В фибриллах коллагена II-го типа все мономеры были ориентированы таким образом, чтобы C-концы указывали на растущую верхушку [ Fertala ea 1994 ].
Недавно для исследования задержки роста фибрилл, ассоциируемых с помощью нейтрализации и нагревания растворов экстрагируемого холодными кислотными буферами коллагена была использована трансформирующая инфракрасная спектроскопия Фуриера ( FTIP ) [ Veis ea 1994 ].
Результаты соответствуют заключению, по которому при повышении температуры тройная спираль уплотняется или становится жесткой, а затем вновь релаксирует при образовании фибрилл [ Veis ea 1994 , George ea 1991 ].
Смотрите также: