Анкирин: взаимодействие с Na,K-ATPaзой
В эпителиальных тканях локализация ион-транспортирующих белков в базальной или апикальной части плазматической мембраны определяет направление транспорта ионов через эпителий. В функционировании как секретирующих, так и абсорбирующих эпителиальных тканей существенную роль играет Na,K-ATPaзa .
В хороидном плексусе (однослойный секреторный эпителий, выстилающий желудочки мозга) Na,K-ATPa3a расположена в апикальной мембране, где она регулирует выделение Na+ и секрецию цереброспинальной жидкости .
Напротив, в клетках абсорбирующего эпителия почек Na,К-ATPaзa локализована в базолатеральной мембране, где она участвует в переносе Na+ из клетки в межклеточное пространство, являясь движущей силой для реабсорбции Na+ из протока нефрона через эпителий в кровоток.
Локализация Nа,К-АТРазы в соответствующих областях мембраны обеспечивается адресной доставкой вновь синтезированного фермента из аппарата Гольджи и удалением неправильно расположенных молекул фермента с последующей их деградацией. Это становится возможным за счет взаимодействия Na,K-ATPaзы с белками мембранного цитоскелета актином и фодрином . Показано, что Na,K-АТРаза выделяется совместно с этими белками в виде белкового комплекса [ Marrs J.A. et al., 1993 ].
В клетках хороидного плексуса анкирин , фодрин , актин , миозин и альфа-актинин локализованы главным образом в апикальной мембране и связываются предпочтительно с Na,К-АТРазой, но эти белки не обнаруживаются вблизи базолатеральной мембраны, где находится белок полосы 3 [ Alper S.L. et al., 1994 ].
Аналогичные результаты были получены при исследовании двухслойного пигментного эпителия сетчатки . Апикальная поверхность этого типа эпителия не выстилает полость, а находится в тесном контакте с фоторецепторными клетками, причем контакты образованы некадгериновой системой клеточной адгезии (N-CAM) . Показано, что Na,K-ATPaзa удерживается в апикальной части плазматической мембраны клеток сетчатки благодаря ее связыванию с анкирином и фодрином [ Gundersen D. et al., 1991 , Gundersen D. et al., 1993 ], а также с еще не охарактеризованным кадгерин-подобным белком [ Huotary V. et al., 1995 ].
Базолатеральная локализация Na,K-ATPaзы в клетках почек также обусловлена ее связыванием с белками примембранного цитоскелета . Показано, что Na,K-ATPaзa экстрагируется из культуры клеток почек MDCK совместно с анкирином и фодрином в виде белкового комплекса [ Nelson W.J. and Hammerton R.W.J., 1989 ].
Характерно, что Na,K-ATPaзa, фодрин и анкирин совместно располагаются в базолатеральной мембране эпителиальных клеток почек только после того, как клетки достигнут зрелого состояния. До этого момента все перечисленные белки диффузно распределены в клетке: Na,K-ATPaзa в плазматической мембране, фодрин в цитоплазме, а анкирин ассоциирован как с плазматической, так и с внутренними мембранами [ Morrow J.S. et al., 1989 ]. Поляризованное распределение анкирина и Nа,К-АТРазы значительно нарушается при ишемическом повреждении почек и восстнаавливается после устранения повреждения [ Siegel N.J. et al., 1994 ].
Анкирин, фодрин, Na,K-ATPaзa и адгезионная молекула нейроглиан также совместно локализуются в базолатеральной части мембраны клеток слюнных желез дрозофилы [ Dubreuil R.R. et al., 1997 ].
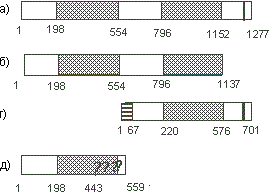
Анкирин взаимодействует с альфа-субъединицей Nа,К-АТРазы [ Morrow J.S. et al., 1989 ]. По-видимому, на молекуле эритроцитарного анкирина имеется два участка связывания Na,K-ATPaзы: один находится в N-концевом мембраносвязывающем домене , а второй - в спектринсвязывающем домене [ Davis J.Q. and Bennett V., 1990 ]. При исследовании связывания Na,K-ATPaзы изолированными доменами эритроцитарного анкирина было отмечено слабое связывание фермента с любым из этих доменов. Предполагается, что для связывания с высоким сродством, характерного для интактного анкирина, необходим контакт фермента с обоими доменами [ Davis J.Q. and Bennett V., 1990 ].
Изучение связывания Nа,К-АТРазы с Ank G190 выявило на молекуле анкирина два участка связывания фермента: один в области 12 последних тандемных повторов , а второй - в спектрин-связывающем домене [ Thevananther S. et al., 1998 ].
Таким образом, взаимодействие анкирина с интегральными мембранными белками обеспечивается несколькими участками связывания и может происходить при участии сложных структурных детерминант.
В экспериментах in vitro Na,K-ATPaзa и 43 кДа цитоплазматический домен белка полосы 3 конкурируют за ассоциацию с анкирином , хотя заметных гомологии в их первичной структуре не обнаружено [ Morrow J.S. et al., 1989 ]. In vitro анкирин связывается с Nа,К-АТРазой в молярном соотношении 1:4 (по другим данным - в соотношении 1:20 [ Nelson W.J. and Veshnock P.J., 1987 ]) с высоким сродством (Kd=2,5-25 нМ) [ Morrow J.S. et al., 1989 , Devarajan P. et al., 1994 ]), она вытесняется из комплекса цитоплазматическим доменом белка полосы 3 [ Morrow J.S. et al., 1989 ].
In vitro два из пяти цитоплазматических доменов альфа-субъединицы Na,K-ATPaзы (II и III) взаимодействуют с эритроцитарным анкирином и анкирином G , причем домен II (аминокислотные остатки 140-290) проявляет большее сродство к анкирину, чем домен III (аминокислотные остатки 345-784) [ Devarajan P. et al., 1994 ]. Первичная структура домена II высококонсервативна между видами и изоформами фермента и гомологична таковой в Н,К-АТРазе (75% гомологии), а также ограниченной последовательности (195-247 аминокислотные остатки) в Са-AТРазе плазматических мембран [ Devarajan P. et al., 1994 ].
Гомологии с другими анкиринсвязывающими интегральными белками не обнаружено.
Проведенные исследования показали также, что во взаимодействии с анкирином участвуют аминокислотные остатки 142-166 (последовательность Ser-Tyr-Tyr-Gln-Glu-Ala-Lys-Ser-Ser-Lys-Ile-Met-Glu-Ser-Phe-Lys-Asn-Met- Val-Pro-Gln-Gln-Ala-Leu-Val) II цитоплазматического домена альфа- субъединицы Nа,К-АТРазы. Рекомбинантные пептиды глутатион-S-трансферазы , включающие эти 25 аминокислотных остатков, специфически связываются с очищенным анкирином с Kd=118+50 нМ. Этот минимальный анкиринсвязывающий участок содержит петлю, состоящую из 7 аминокислотных остатков с заряженной гидрофильной поверхностью, которая с двух сторон оканчивается двойной бета-структурой.
Сравнение минимальных анкиринсвязывающих последовательностей в р53 , CD44 , InsP3R (InsP3-рецептоpом) и нейрофасцине позволяет заключить, что прочность и специфичность связывания анкирина достигается за счет взаимодействия петель, состоящих из 5-7 аминокислотных остатков, с концами бета-шпилек в анкириновых повторах [ Zhang Z. et al., 1998 ].
Взаимодействие цитоплазматического домена III альфа-субъединицы Nа,К-АТРазы с анкирином обеспечивается кластером из 4 аминокислотных остатков (Ala-Leu-Leu-Lys). Предполагается, что в результате конформационных изменений, происходящих в молекуле Nа,К-АТРазы при связывании ее с анкирином, становятся доступными и другие участки связывания. Сходная последовательность (Ala-Leu-Leu-Leu-Lys), обнаруженная в цитоплазматическом домене белка полосы 3 , также является необходимой для связывания анкирина с этим белком [ Jordan C. et al., 1995 ].
Смотрите также: