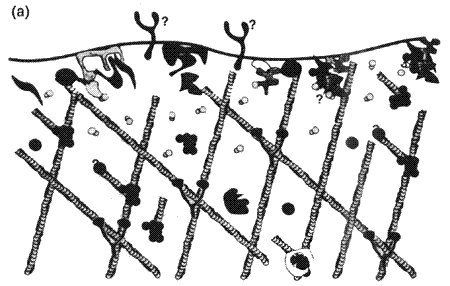
Парамиксовирусы: структура
Вирусная частица - шарообразная (иногда плеоморфная или нитевидная), с диаметром 150-300 нм ( рис. 1.6 ). Наружная липопротеидная оболочка содержит два трансмембранных гликопротеида, образующих на внешней стороне вирусной частицы выступы или шипы длиной 8-12 нм. Один из гликопротеидов, имеющий функцию белка прикрепления, обозначается у разных представителей семейства либо Н белок , либо HN белок , либо G белок (от англ. hemagglutinin, или hemagglutinin-neuraminidase, или glycoprotein). Другой белок, обеспечивающий слияние вирусной оболочки с клеточной мембраной, обозначается F белок (от англ. fusion).
У представителей Paramyxovirinaeбелки Н или HN в составе вирусной частицы представлены тетрамерами, a F - тримерами. Белок прикрепления (HN - у Respirovirus и Rubulavirus и Н - у Morbillivirus ) представляет собой мембранный гликопротеид 2-го типа. Он закреплен в липидном слое N-концевой частью. Белок HN при контакте вируса с клеткой связывается с остатками сиаловой кислоты в олигосахаридах, входящих в состав поверхностных клеточных гликопротеидов и гликолипидов. Кроме того, он обладает нейраминидазной активностью, т.е. отщепляет концевые остатки сиаловой кислоты от олигосахаридов в составе клеточных и вирусных белков. Устранение сиаловых остатков, являющихся рецепторами, с которыми вирус способен связываться, предотвращает агрегацию вирусных частиц и сорбцию агрегатов на поверхности зараженной клетки, что обеспечивает эффективное распространение вируса от клетки к клетке.
Полипептидная цепь белка HN включает 565-582 а.о. у разных вирусов и имеет 4-6 сайтов гликозилирования. Тетрамер белка HN состоит из двух нековалентно связанных димеров, в каждом из которых мономеры соединены дисульфидной связью. Белок прикрепления у вирусов рода Morbillivirus (Н) имеет значительное сходство с белком HN у Respirovirus и Rubulavirus по последовательности аминокислот, но не обладает нейраминидазной активностью. Это отличие обусловлено тем, что клеточным рецептором для вирусов рода Morbillivirus является не концевая сиаловая кислота в олигосахаридах, а присутствующий в плазматической мембране кофактор комплемента CD46 .
Белок G у Pneumovirinae резко отличается от белков Н и HN . Он содержит 280-299 а.о. у разных вирусов и имеет в своем составе не только N-связанные, но и О-связанные олигосахариды, причем степень гликозилирования белка G очень высока.
Белок F является гликопротеидом 1-го типа, он закреплен в липидном слое гидрофобным трансмембранным доменом в С-концевой части молекулы и С-концевым гидрофильным участком длиной 40-80 а.о. с внутренней стороны липидного слоя. Белок F состоит из двух субъединиц, соединенных дисульфидной связью . Он синтезируется как единая полипептидная цепь, содержащая 540-580 а.о. у разных вирусов, и расщепляется клеточной протеазой на субъединицы F1 и F2. У вирусов родов Respirovirus и Rubulavirus обе субъединицы гликозилированы, а у Morbillivirus - только F2. Гидрофобный N-концевой участок F1 инициирует слияние липидного бислоя вирусной частицы с таковым клеточной стенки. У большинства вирусов семейства Paramyxoviridae для слияния вирусной оболочки с клеточной мембраной необходимо совместное участие белков F и HN (или Н), но у вируса кори и вируса РСВ белок F осуществляет эту функцию самостоятельно, без участия белка прикрепления.
У вирусов рода Rubulavirus оболочка помимо белков F и HN содержит небольшой негликозилированный трансмембранный белок SH .
Внутренний листок липопротеидной оболочки вирусной частицы образован белком М (матриксный или мембранный белок). Белок М, наиболее обильно представленный в вирусной частице, представляет собой полипептид, содержащий от 345 до 371 а.о. у разных вирусов. Белок слабо гидрофобен, он ассоциирован как с липидным слоем, так и с нуклеокапсидом. У некоторых вирусов он фосфорилирован.
Внутренняя структура вирусной частицы, нуклеокапсид , представляет собой спиральный рибонуклеопротеид, свернутый во вторичную шарообразную структуру. Нуклеокапсид содержит геномную РНК и три белка: главный белок нуклеокапсида ( N ), фосфопротеид ( Р ) и РНК-зависимую РНК-полимеразу (L). У вируса Сендай (парамиксовирус мышей , прототипный для рода Respirovirus ) в состав нуклеокапсида входят 2500 молекул белка N, 300 молекул белка Р и 50 молекул белка L. Длина одного витка спирали нуклеокапсида составляет у разных вирусов от 5,8 до 7 нм ( рис. 1.6 ). Белок N содержит у разных вирусов от 489 до 553 а.о. Его N-концевой консервативный домен, составляющий 80% молекулы, образует плотную глобулу. Именно он взаимодействует с РНК и определяет общую спиральную структуру нуклеокапсида. Каждая молекула белка N связывается с шестью нуклеотидами вирусной РНК. Вариабельный С-концевой участок молекулы белка N сильно фосфорилирован и содержит главные антигенные участки белка N.
Фосфопротеид Р является компонентом полимеразного комплекса. Функционально активный полимеразный комплекс содержит 1 молекулу белка L и от 4 до 10 молекул белка Р. Последний необходим для ассоциации белка L с вирусной РНК и для инициации транскрипции. Кроме того, белок Р участвует в инкапсидации вирусной РНК.
Самый большой вирусный белок L (около 2200 а.о.) осуществляет синтез вирусной РНК, включая инициацию, элонгацию и терминацию, а также кэпирование 5'- и полиаденилирование З'-конца мРНК.
Смотрите также: