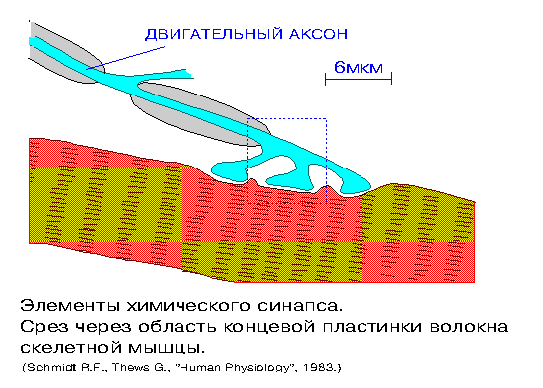
ДНК топоизомераза I белок E.coli
ДНК-топоизомеразы I являются мономерными белками, релаксируют ДНК без затраты энергии путем внесения одноцепочечных разрывов. ДНК-топоизомеразы II функционируют в виде димеров, осуществляя ATP-зависимое расщепление обеих цепей ДНК с последующим переносом цепей через разрыв и его лигированием ( рис. I.3 ).
Для внесения одноцепочечного разрыва в ДНК все ДНК- топоизомеразы используют остаток Tyr, который осуществляет нуклеофильную атаку фосфатной группы ДНК с образованием фосфотирозина. В результате ферменты оказываются ковалентно связанными с 5'- или 3'-концами ДНК в одноцепочечном разрыве. Образование такой ковалентной связи исключает необходимость затраты энергии при восстановлении фосфодиэфирной связи в одноцепочечном разрыве на заключительных стадиях реакции. У ДНК- топоизомераз типа I имеется один каталитический остаток Tyr на молекулу мономерного белка, тогда как димеры ДНК-топоизомераз II содержат по одному каталитическому остатку на каждую субъединицу, что обеспечивает создание ступенчатого двухцепочечного разрыва в молекуле релаксируемой ДНК.
Топоизомераза I была открыта в 1969 г. ( Wang J.C., 1971 ). В настоящее время топоизомеразы типа I найдены почти во всех классах живых организмов. В ходе своей работы топоизомеразы типа I вносят разрыв лишь в одну из цепей двойной спирали. Топоизомеразы типа I из прокариотических клеток способны вызывать релаксацию отрицательно, а из эукариотических - иногда и положительно сверхспирализованной кольцевой замкнутой ДНК. Для своей работы они не требуют никаких кофакторов. Внося разрыв в одну из цепей двойной спирали, фермент ковалентно пришивается к одному из концов цепи, запасая в образованной связи энергию, необходимую для последующего воссоединения этой цепи.
ДНК-топоизомераза IA релаксирует ДНК, содержащие только отрицательные супервитки, работает в присутствии ионов Mg2+ и ковалентно соединяется с 5'-концами ДНК в образующихся врeменных одноцепочечных разрывах. Это сближает ДНК-топоизомеразы IA и II между собой, что подтверждено структурными исследованиями.
ДНК-топоизомеразы IB способны релаксировать ДНК как с положительными, так и отрицательными супервитками, не требуют для своего функционирования ионов металлов и взаимодействует ковалентно с 3'-концами ДНК. ДНК-топоизомеразы IB найдены исключительно в клетках эукариот (за единственным исключением вируса вакцины).
В клетках человека ДНК-топоизомераза IB/III специфически ингибируется камптотецином (camptothecin) , который рассматривается в качестве перспективного противоопухолевого препарата. Это соединение взаимодействует преимущественно с ковалентным комплексом топоизомераза I-ДНК, что подавляет реакцию восстановления фосфодиэфирной связи и освобождение фермента из комплекса. В результате происходит быстрое накопление двухцепочечных разрывов ДНК и вступление клеток в апоптоз.
Топоизомеразы типа I, возможно, вызывают изменчивость генома у эукариот . Эти ферменты могут разрезать одноцепочечную ДНК в районах с потенциалом к внутрицепочечному спариванию [Been, M.D, 1984 ] и остаются связанными с 3'- концом. Они могут присоединять этот конец к 5'- концу одноцепочечной или двуцепочечной ДНК [Been,M.D, 1981 , Halligan, B.D. et al. 1982]. Короткие последовательности, вовлеченные в вырезание провируса SV40 из генома клеточной линии крысы [Bullock, P. et al. 1984], похожи на сайты узнавания топоизомеразы [Edwards, K.A. et al. 1982],также некоторые сайты вырезания SV40 совпадают с сайтами, по которым топоизомераза режет in vitro [Bullock, P. et al. 1985]. Топоизомеразы - ферменты, изменяющие число зацеплений в ДНК ; топоизомеразы типа I изменяют число зацеплений последовательно на единицу, топоизомеразы типа II изменяют число зацеплений последовательно на два. См. Топоизомераза II ядерного матрикса
Смотрите также: