Ишемия головного мозга: молекулярные механизмы восстановления
При восстановлении эффективного кровотока до формирования необратимых некротических повреждений в ткани мозга начинается стереотипный восстановительный процесс.
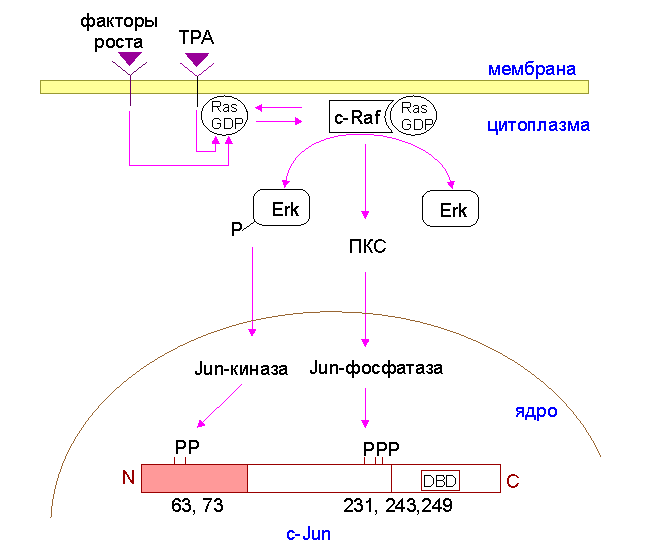
Промежуточные метаболиты системы оксидантного стресса , являющиеся вторичными мессенджерами, инициируют каскад жизнеспасающих реакций в ишемизированной ткани [ Kogure K., Yamasaki Y. 1996 ]. Их фосфорилирование служит сигналом к экспрессии генов раннего реагирования в пораженных нейронах и глиальных клетках ( схема 7.1 и рис. 7.1 ), которая происходит даже в условиях угнетенного (вследствие нарушений чрезмембранного транспорта аминокислот и разрушения рибосом) синтеза протеинов.
Экспрессия генов раннего реагирования вызывает образование таких факторов транскрипции , как индуктор фактора роста нервов A (NGFI-A) , содержащий цинк-пальцевый домен (zinc finger) ; белки fos , jun , c-myc генных семейств, содержащие leucin zipper и helix-loop-helix домены; транскрипционный фактор рецептора стероидного гормона NGFI-B . Факторы транскрипции могут играть важную роль в продукции острофазных стресс-белков . Так, экспрессия цинк-пальцевых генов приводит к синтезу стресс-белка HSP72 , предположительно обладающего нейропротективными свойствами. Ферменты супероксиддисмутаза , каталаза , орнитиндекарбоксилаза также отнесены к стресс-белкам , хотя их роль еще до конца не ясна [ Kogure K., Yamasaki Y. 1996 ].
Экспрессия генов раннего реагирования , индукция образования факторов транскрипции и стресс-белков могут повышать резистентность пораженных клеток мозга к вызванным ишемическим изменениям. Основополагающим механизмом, лежащим в основе приобретения клеткой толерантности к вторичной ишемии, является снижение чувствительности внутриклеточных рецепторов системы сигнальной трансдукции. Однако, если этот организованный ответ не позволяет клеткам мозга избежать предстоящей смерти, включается второй уровень защиты - активируется синтез разнообразных трофических факторов и рецепторов к ним на поверхности мембран клеток-мишеней ( схема 12.1 ).
Экспериментальными исследованиями [ Kokaia Z., Zhao Q. 1995 , Lindvall O., Ernfors P. 1992 , Takeda A., Onodera H. 1992 ] установлено, что кратковременная ишемия мозга, не приводящая к повреждению клеток, сопровождается повышенной активностью мРНК, кодирующей нейротрофины - фактор роста нервов (NGF) и фактор роста, выделенный из головного мозга (BDNF) . Экспрессия нейротрофина-3 (NT-3) при этом кратковременно снижена. Более длительная фокальная ишемия вызывает последовательное нарастание синтеза нейротрофинов с максимумом через 12 ч после развития инсульта и последующей нормализацией ко 2-м суткам [ Takami K., Kiyota Y. 1993 ]. Степень увеличения синтеза BDNF коррелирует с экспрессией гена раннего реагирования c-fos [ Kokaia Z., Zhao Q. 1995 ]. Однако, если содержание BDNF повышается только в области, окружающей ишемизированную ткань, экспрессия c-fos определяется и в ядерной зоне ишемии . Активация синтеза BDNF подавляется гипергликемией и гиперкапнией [ Uchino H., Lindvall O. 1997 ].
Клинические исследования [ Скворцова В.И., Клюшник Т.П. 1999 , Скворцова В.И., Мясоедов Н.Ф. 2000 , Skvortsova V.I., Gusev E.I. 2000 , Гусев Е.И., Скворцова В.И. 2001 ] подтверждают факт повышения концентрации NGF в цереброспинальной жидкости больных в первые 12 ч после развития каротидного ишемического инсульта, выраженность которого имеет прогностическую значимость.
Активированные астроциты и, возможно, микроглиальные клетки , находящиеся поблизости от пострадавших нейронов, поддерживают в них восстановительные процессы [ Kogure K., Yamasaki Y. 1996 ]. Так, уже через 10 мин после индукции глобальной церебральной ишемии зафиксирован синтез основного фактора роста фибробластов (bFGF) и рецепторов к нему в астроцитах [ Takami K., Iwane M. 1992 , Takami K., Kiyota Y. 1993 ] и нейронах [ Endoh M., Pulsinelli W.A. 1994 ], причем основным источником трофического фактора являются глиальные клетки . При экспериментальном инсульте накопление bFGF происходит преимущественно в реактивных астроцитах [ Finklestein S.P., Apostolides P.J. 1988 ] и лишь при отдалении от центра ишемии выявлено в нейронах [ Kumon Y., Sakaki S. 1993 ].
При стойкой фокальной ишемии мозга зарегистрирована индукция сосудистого эндотелиального фактора роста (VEGF) в нейронах, астроцитах, микроглиальных и эндотелиальных клетках, максимальная по выраженности через 18 ч после развития инсульта и сохраняющаяся на протяжении 2 нед [ Kovacs Z., Ikezaki K. 1996 ]. При преходящей фокальной ишемии отмечено раннее повышение синтеза VEGF (с максимумом через 13 ч от начала рециркуляции) с последующей его нормализацией к концу 1-х суток [ Hayashi Т., Abe K. 1997 ].
В течение первых дней экспериментального инсульта установлены увеличенная продукция инсулин-зависимого фактора роста II (IGF-II) и рецепторов к нему в нейронах ишемизированной области мозга, в том числе ее ядерной зоны [ Schmidt-Kastner R., Bedtird A. 1997 ], и повышенный уровень инсулин-зависимого фактора роста I (IGF-I) , который коррелирует с выраженностью реактивного глиоза [ Gluckman P., Klempt N. 1995 , Lee W.H., Clemens J.A. 1992 ].
В процессах постишемического восстановления принимают участие и гены, экспрессия которых вызывает синтез ростовых фосфопротеинов (например, GAP-43) [ Schmidt-Kastner R., Bedtird A. 1997 , Tagaya M., Matsuyama Т. 1995 ]. Доказано, что повышенная продукция GAP-43 , тесно связанного с процессами пластичности ткани мозга, синаптогенезом, коррелирует с регрессом неврологических нарушений и нормализацией поведения у экспериментальных животных, перенесших инсульт [ Stroemer R.P., Kent T.A. 1995 ].
Морфологическая и функциональная пластичность ишемизированной ткани мозга также определяется выработкой микротубулин-связанного протеина-2 (MAP-2) [ Dawson D.A., Hallenbeck J.M. 1996 , Inuzuka Т., Tamura A. 1990 , Pettigrew L.C., Holtz M.L. 1996 ]. Степень постишемической экспрессии MAP-2 в нейронах отражает их толерантность к ишемии и способность к репаративным процессам [ Okawa M., Halaby I. 1995 ].
Трофические факторы наряду с аутокринной стимуляцией собственных рецепторов индуцируют дальнейшие сигнальные каскады, приводящие к синтезу регуляторных протеинов, которые предотвращают индукцию апоптоза и способствуют клеточному жизнеобеспечению.
Одако при массивном ишемическом поражении мозга, сопровождающемся грубым энергетическим дефицитом, усиление трофического обеспечения и тканевой пластичности оказывается недостаточным для спасения поврежденных клеток.
Смотрите также: